精准基因编辑是生物育种的核心技术,也是培育优良家畜品种的关键,但传统CRISPR/Cas9技术因Cas9序列长、依赖双AAV载体递送编辑器和供体HDR模板,且制备编辑动物需显微注射造成胚胎损伤,成为大动物精准育种的限速瓶颈。
2026年3月17日,内蒙古大学杨磊、李光鹏教授与同济大学高绍荣院士团队再度携手攻关,在Nature子刊《Cell Discovery》(IF=13)发表研究论文,通过改造获得高效低脱靶的微型IscB#/ωRNA#编辑工具,构建出All-in-One全新AAV递送体系,实现受精卵无显微操作的直接精准编辑,成功获得抗热应激SLICK基因编辑牛,为反刍家畜精准育种开辟了极简高效新路径。

原文链接:https://doi.org/10.1038/s41421-026-00871-y
一、研究突破:三大技术创新打造家畜精准编辑系统
本研究以构建极简式基因编辑技术体系为目标,从工具、载体、递送方式三方面实现突破,打造出适配家畜育种的精准编辑系统:
1.改造微型编辑工具,兼顾高效与低脱靶。以Cas9祖先蛋白IscB为基础,截短其TID基序筛选出高效变体IscB#,同时截短ωRNA茎环结构获得ωRNA#,构建的IscB#/ωRNA#在细胞中编辑效率提升至73%,且高预测脱靶位点的脱靶效应大幅降低。
2.开发All-in-One递送,突破容量限制。构建整合IscB#/ωRNA#与最长2.5kb自切割HDR模板的单AAV载体,提升同源定向修复效率,解决了传统技术需双AAV递送的难题,为家畜基因片段敲入、外显子替换提供核心工具。
3.建立无显微操作孵育,保护胚胎完整性。利用AAV穿透胚胎透明带的特性,实现受精卵不去除透明带、无显微注射的直接编辑,避免胚胎机械损伤,有效提升囊胚形成率与活体动物出生率。
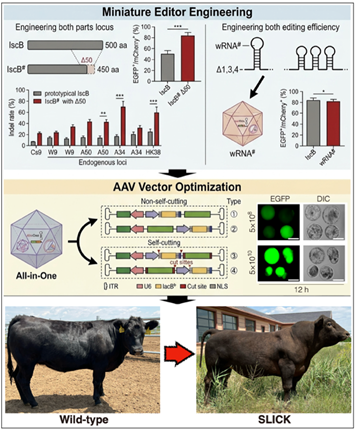
「All-in-One」全新生物育种路径
二、跨物种验证:从模式动物到肉牛的成功落地
研究团队先完成小鼠模型有效性验证,靶向酪氨酸酶(Tyr)基因实现近93%的白化表型敲除,该技术单基因编辑效率与传统显微注射相当,还可实现双基因高效敲除,囊胚形成率也从65.3%提升至85.4%。随后团队将技术体系拓展至肉牛育种,优化AAV孵育条件后,成功实现牛催乳素受体(PRLR)基因外显子的精准替换,编辑囊胚移植后获得2头犊牛,出生率与普通体外受精IVF胚胎持平,其中1头安格斯牛健康存活至成年,表现出短毛的SLICK表型,且在预测脱靶位点无脱靶效应、编辑工具无残留,团队也借此实现了全球首个批准上市CRISPR编辑SLICK牛的一步法快速创制,成功获得无脱靶的精准编辑种质,充分验证了该技术的实用性。
三、核心价值:推动家畜生物育种向高效化、产业化升级
这项研究的价值,不仅在于成功开发出微型编辑工具,更在于彻底打破了传统CRISPR技术在育种中的应用局限,为反刍动物提供了“All-in-One”的路径支撑,推动生物育种向高效、便捷方向升级。培育的SLICK抗热应激牛完全符合安全认证标准,为我国基因编辑家畜的产业化应用奠定了种质基础。该SLICK品种能显著提升高温地区牛的养殖存活率与生产效率,对缓解气候变暖对畜牧业的影响、保障肉奶供给具有重要的现实意义。
杨磊教授、李光鹏教授、高绍荣院士为本文共同通讯作者,宋丽爽讲师、刘雪霏助理研究员、狄安琪博士、吴迪博士、白春玲副教授为共同第一作者。该研究获教育部U40计划、国家自然科学基金、科技创新2030重大项目、内蒙古科技突围等项目资助。内蒙古大学与同济大学此前已在《Nature Biotechnology》发表牛羊单倍体育种重要成果,此次研究进一步巩固了两家单位在生物育种领域的国际领先地位。目前,团队已就该技术获批两项专利,为后续产业化应用提供了知识产权保障。
编辑:宋丽爽
审校:白春玲
审核:杨磊
终审:徐军